Esta es la primera vez que el CHMP adopta una opinión positiva para ampliar la indicación de una vacuna frente al VRS en personas mayores de 18 años que no sean mujeres embarazadas.
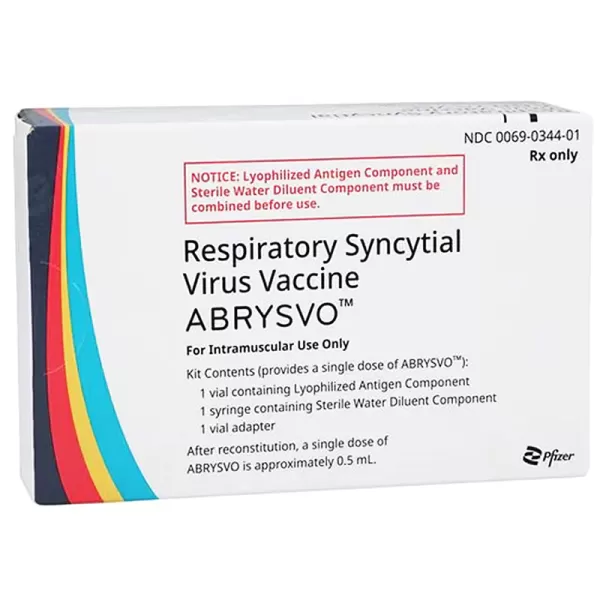
Pfizer Inc. (NYSE: PFE) ha anunciado que el Comité de Medicamentos de Uso Humano (CHMP, por sus siglas en inglés) de la Agencia Europea de Medicamentos (EMA) ha adoptado una opinión positiva para su vacuna bivalente (RSVPreF) para la prevención de la enfermedad del tracto respiratorio inferior (ETRI) causada por el Virus Respiratorio Sincitial (VRS) en personas de 18 años de edad y mayores1.
Se trata de la primera vacuna frente al VRS indicada para adultos de 18 años y mayores, que no sean mujeres embarazadas, que recibe la opinión positiva del CHMP. De aprobarse en Europa por la Comisión Europea (CE), la vacuna frente al VRS de Pfizer ofrecería la cobertura más amplia para la prevención de esta enfermedad en adultos, cuya indicación actualmente incluye a los mayores de 60 años*.


:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/2F64NXXUXVGLZLF2BFL5JJ2CYM.jpg)

:quality(75)/cloudfront-us-east-1.images.arcpublishing.com/elcomercio/XKFWJXYMRVFHLPW5M3DCVMKOAU.jpg)