Actualización de la enfermedad por herpes zóster mediante revisión de casos clínicos
| Introducción |
El herpes zóster (HZ) es una entidad infecciosa y neurológica prevalente, cuya incidencia ha aumentado en las últimas dos décadas. Al menos el 20-30% de la población y hasta el 50% de los mayores de 85 años se verá afectado por HZ, aunque esto está cambiando con la vacunación.
Los dermatólogos suelen diferir en sus enfoques de manejo, y las estrategias de vacunación para HZ son inconsistentes a pesar de las diversas recomendaciones. Además, las políticas de control de infecciones en entornos sanitarios para pacientes y personal con o expuesto a HZ a menudo son incomprendidas, están desactualizadas o mal descriptas en las directrices institucionales.
Una entidad patológica con estrategias de manejo tan dispares debe aclararse. Esta revisión basada en casos tiene como objetivo ilustrar el manejo y la educación de los pacientes con HZ y sus equipos de atención.
| Casos y revisión |
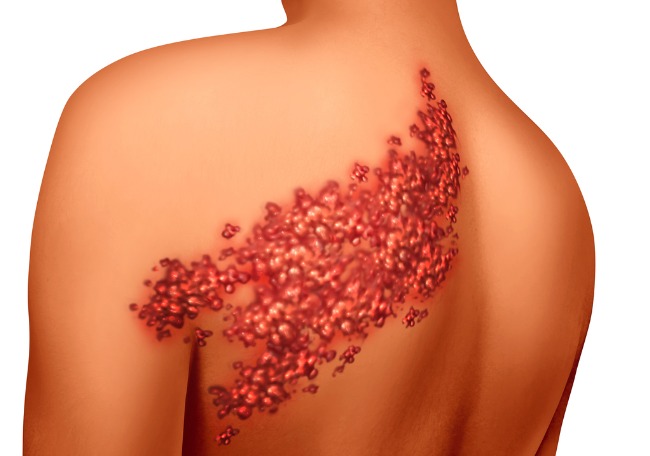
> Hombre de 72 años, por lo demás sano, que presenta pápulas rosadas dolorosas a lo largo de la parte media derecha de la espalda desde hace 3 días. Creía haber sido mordido por una araña o una garrapata y pregunta "cómo lo atrapó".
Una brecha sustancial en el manejo del HZ radica en el uso de su verdadera fisiopatología para acotar los diagnósticos diferenciales y evitar pruebas, tratamientos e inquietudes innecesarias. Zoster es el término griego para "cinturón" o "faja", y "culebrilla" proviene del latín cingulum que significa "rodear el cuerpo"; ambos ejemplifican la clásica distribución torácica papulovesicular dermatómica dolorosa de más de la mitad de los casos de HZ.
El virus varicela-zoster (VZV), virus del herpes humano tipo 3, es responsable de infecciones por HZ y varicela primaria y parte de la subfamilia de α-herpesvirus con capacidad de permanecer latente en el tejido neural.
Todos los pacientes con HZ han incurrido en alguna versión de exposición al VZV, generalmente en la niñez, ya sea por contacto con la enfermedad o vacunación.
Para el primero, la infección inicial puede haberse manifestado como papulovesículas cutáneas difusas autolimitadas, raramente con complicaciones sistémicas, o quizás hallazgos sutiles, incluso poco recordados por el paciente. Después de 1995, la actual población de niños y adultos jóvenes puede haber recibido en cambio la vacuna viva atenuada contra VZV.
El VZV puede quedar latente en la raíz espinal o ganglios de los nervios craneales luego de la exposición original. A lo largo de la vida, pueden ocurrir reactivaciones subclínicas por el contacto comunitario con el virus, aumentando la inmunidad.
Para el inmunocompetente, este equilibrio se mantiene en la edad adulta hasta que se alcanza la edad de vacunación para HZ o, si no se alcanza un nivel umbral de inmunidad, hasta que sobreviene el HZ. Los contribuyentes más comunes a esta inmunidad menguante son la edad, la inmunosupresión intrínseca o farmacológica, o la protección inmune original silenciada luego de infección o vacunación.
> Mujer embarazada de 30 años (28 semanas) con erupción compatible con una infección aguda por varicela con vesículas difusas en todo el cuerpo. Su hija nace a término sin complicaciones, pero a los 10 meses de vida desarrolla una erupción herpética que involucra la región T3.
Si una mujer desarrolla varicela durante el embarazo, técnicamente el feto está experimentando su primera exposición al VZV al mismo tiempo.
En los primeros dos trimestres el riesgo de complicaciones virales congénitas por varicela es alto (~25%), incluyendo baja tasa de natalidad, parto prematuro, y síndrome de varicela congénita, y más tarde en el embarazo, la exposición materna primaria al VZV puede causar varicela neonatal.
Además, la transmisión primaria de VZV en el tercer trimestre o la infección primaria por VZV en el primer año de vida llevan a un mayor riesgo de HZ precoz (< 4 años de edad), por la incipiente inmunidad celular y humoral del feto y el lactante y la respuesta inmune silenciada a la infección.
El HZ en niños también puede presentarse por verdadera inmunosupresión, por malignidad, medicamentos inmunomoduladores (corticoides sistémicos o azatioprina), cirugía, trauma y trastornos autoinmunes como lupus, artritis reumatoide, enfermedad intestinal inflamatoria, asma, VIH y diabetes tipo 1.
En general los casos de HZ pediátrico son raros, especialmente luego de la vacunación para el VZV primario. La presentación suele ser menos sintomática y con menos riesgo de neuralgia post-herpética (NPH) que en adultos.
Los niños vacunados tienen 72% a 79% menos de probabilidades de presentar HZ en la infancia que los no vacunados. Con el tiempo, con menos infecciones primarias por VZV de tipo salvaje y asumiendo altas tasas de vacunación en la comunidad, los niños vacunados serán adultos con un riesgo reducido de HZ.
> Un hombre afroamericano de 24 años con apariencia enferma se presenta con vesículas tensas que se extienden rápidamente sobre el cuerpo. Está febril y no puede caminar debido a lesiones dolorosas en regiones plantar y genital. Es internado y tratado con aciclovir intravenoso. Se revela el diagnóstico de infección concurrente por VIH.
Algunas presentaciones de HZ sugieren una infección diseminada que requiere además de internación para tratamiento, la evaluación de la inmunosupresión si hay factores de riesgo. El HZ diseminado se define por al menos 20 lesiones vesículo-bullosas generalizadas fuera de los dermatomas primarios y adyacentes, con lesiones en evolución 1 a 2 semanas después de la presentación primaria. Suele haber dolor prominente y otros signos sistémicos que imitan la viremia primaria por VZV, y con mayor riesgo de enfermedad pulmonar, neurológica y complicaciones secundarias por infección bacteriana.
Los pacientes con VIH y malignidad hematológica o tratamiento inmunosupresor, así como receptores de trasplantes, tienen mayor riesgo de diseminación y sus presentaciones pueden variar o incluso evolucionar a una enfermedad crónica.
La incidencia de HZ está disminuyendo en pacientes con VIH por la evolución de la terapia antirretroviral, pero debido a la supresión de las células T inmunes al VZV, aún es frecuente y muestra síntomas graves, como la presentación genital. Además, los pacientes inmunosuprimidos pueden tener resistencia al aciclovir y experimentar NPH más severa, particularmente cuando HZ se presenta en la distribución dermatómica V1.
> Mujer de 83 años con pápulas rosadas dolorosas, pruriginosas y costrosas de rápida evolución en su mejilla derecha. No está segura de recordar su lista de medicamentos.
El diagnóstico diferencial de HZ es amplio dependiendo de los síntomas, particularmente si las clásicas papulovesículas dermatómicas no están presentes de forma aguda. El dolor prodrómico puede simular un evento miocárdico, accidente cerebrovascular, émbolo pulmonar, cólico renal, apendicitis, colecistitis, glaucoma de ángulo agudo y costocondritis, entre otros.
El zoster sine herpete (sin afectación de la piel) es un diagnóstico de exclusión cuando las condiciones antes mencionadas son parte del diferencial. Los imitadores cutáneos del HZ incluyen otras erupciones herpéticas como el virus del herpes tipo 1 o 2 (HSV-1, HSV-2), la superinfección por HSV, VZV avanzado después de la vacunación infantil, entre otras enfermedades virales.
Las etiologías no infecciosas incluyen dermatitis de contacto alérgica, ataque de artrópodos, enfermedad ampollar autoinmune, o, como en este caso, una reacción a la medicación por uso de 5-fluorouracilo tópico.
Las pistas para descartar este amplio diferencial implican señalar la distribución dermatómica; aunque el HZ puede implicar pápulas aberrantes en dermatomas cercanos, la forma debe seguir principalmente a un dermatoma representativo. La reacción en cadena de polimerasa (PCR) para ADN VZV, y el anticuerpo de fluorescencia directa (AFD) siguen siendo las pruebas diagnósticas preferidas cuando se considera necesario.
> Hombre de 62 años con HZ en V1 tratado con antivirales orales. Consulta para preguntar si puede hacer algo más para que las lesiones de HZ sanen más rápidamente y para el dolor. Es profesor universitario de ingeniería y ha estado leyendo sobre prednisona y gabapentina.
La decisión de cómo tratar el HZ puede ser compleja. En casos estándar, se indica una semana de terapia antiviral (aciclovir, valaciclovir o famciclovir) dentro de las 72 h de la erupción primaria, particularmente si el paciente está con dolor significativo, desarrolla nuevas lesiones cutáneas, o tiene riesgo de complicaciones.
La terapia antiviral intravenosa (aciclovir o foscarnet) está indicada ante enfermedad diseminada, compromiso oftalmológico, síntomas neurológicos graves, u otros signos tóxicos. El tratamiento del HZ con antivirales orales reduce el tiempo de resolución de la lesión y la diseminación viral y controla el dolor, pero no previene la NPH. Para niños con riesgo de complicaciones el aciclovir es el único aprobado. No hay indicación de terapia antiviral tópica para el manejo de HZ cutáneo o mucoso.
Los casos leves de HZ solo pueden requerir cuidado localizado de heridas y analgésicos como ibuprofeno o paracetamol. Para síntomas más pronunciados, los corticoides sistémicos pueden reducir el dolor agudo por HZ y mejorar la función diaria; mejoran particularmente la calidad de vida de los pacientes con dolor inicial severo en cualquier sitio o con compromiso neurológico u oftalmológico específico, pero no previenen la NPH.
Los opioides no solo pueden reducir el dolor intenso, sino que tampoco previenen la NPH. El uso de neurolépticos (gabapentina) y antidepresivos tricíclicos (ATC) en el dolor agudo por HZ no está respaldado, a pesar de cierta evidencia de utilidad para los síntomas de NPH.
La primera rama del nervio trigémino (V1) está afectada por el HZ en ~ 10-15% de los casos y puede inicialmente presentarse como signo de Hutchinson en la punta de la nariz. Se indica tratamiento antivírico agudo y posible tratamiento con corticosteroides sistémicos y es conveniente la derivación a oftalmología para diagnosticar y prevenir las complicaciones oculares.
> Mujer de 80 años con antecedente de HZ hace 5 años presentada a dermatología con lo que su médico ha considerado como "zoster recurrente". Ella rse asca y frota activamente su frente durante la consulta.
Este caso describe la disestesia asociada con NPH después del HZ, que se puede confundir con HZ crónico o recurrente. La NPH se define como un dolor o sensación alterada clínicamente relevante que persiste en las regiones afectadas por HZ al menos 3 meses después de la erupción inicial. Puede deberse a un disrupción nerviosa sensorial causada por la replicación del VZV, con inflamación y daño tisular en y alrededor del ganglio de la raíz dorsal o raíz nerviosa craneal correspondiente al dermatoma afectado.
La piel puede mostrar signos crónicos de trauma, superinfección bacteriana y cicatrización por curación de la erupción de HZ y cualquier auto-manipulación debido a disestesia y/o dolor, construyendo la idea errónea de que aún permanece una erupción viral activa. Los síntomas pueden persistir durante más de 1 año.
La única intervención para prevenir la NPH es la vacuna contra el HZ. Aparte de eso, hay innumerables estrategias que pueden ayudar al control del dolor de la NPH, sin consenso particular sobre agentes óptimos, ventana de inicio, o dosificación. La gabapentina puede mejorar la NPH pero no la previene. Tiene inicio de acción lento, muchas opciones de dosis y un abanico de efectos adversos.
Algunos opioides y ATC también controlan el dolor de la NPH, aunque la gabapentina se prescribe más ampliamente. Uno de estos medicamentos debe ser considerado para disminuir la intensidad del dolor por NPH en pacientes con mayor riesgo de síntomas crónicos debilitantes.
Hay alguna evidencia de alivio a corto plazo de los analgésicos tópicos como la lidocaína. La derivación a especialistas en manejo del dolor o neurocirugía para posibles intervenciones, como la administración intratecal de corticosteroides, pueden estar recomendada en casos de NPH recalcitrante.
> La esposa de un paciente está tomando adalimumab para la artritis psoriásica. Consulta si ella y su marido deberían recibir la "vacuna contra el herpes zóster". Ella tiene 52 años y él 61 años. El se aplicó la "vieja vacuna" hace 2 años, pero preguntan por la nueva versión.
La vacunación para HZ tiene como objetivo brindar inmunidad específica contra VZV mediada por células. La vacuna viva atenuada contra HZ de dosis única subcutánea Zostavax fue la primera aprobada por la FDA en 2006 para adultos ≥ 60 años. Zostavax reduce el tiempo de curación de la lesión aguda por HZ y la gravedad de los síntomas si un paciente vacunado desarrolla HZ, y su tasa de prevención de la NPH es del 47,4 al 77% con una eficacia constante inicial, pero con menos efecto preventivo con el tiempo desde la aplicación.
Tiene pocos efectos adversos (reacción local, cefalea), pero como es una vacuna viva, las poblaciones inmunosuprimidas pueden no ser candidatas para su uso. Además, contiene conservantes y está contraindicada en pacientes con anafilaxia a neomicina o gelatina.
En 2017, Shingrix, una vacuna recombinante de subunidades (no viva) con adyuvante, fue aprobada por la FDA y los CDC para personas ≥ 50 años. Es una vacuna intramuscular de dos dosis que se debe administrar con 2 a 6 meses de diferencia y puede administrarse en pacientes que ya han recibido Zostavax si han pasado al menos 2 meses de una vacuna a otra. Ninguna vacuna debe administrarse durante un brote agudo de HZ o mientras un paciente está tomando medicamentos antivirales para cualquier indicación.
La eficacia de Shingrix es mayor, a saber, 84,7 a 97,4% de prevención de HZ y 88,8 a 91,2% de prevención de la NPH, con menor variabilidad o disminución de la eficacia con la edad, y con presentaciones menos graves de HZ y PHN en casos de gran avance. Sus efectos adversos son más pronunciados (dolor localizado, síntomas simil gripe), y las únicas verdaderas contraindicaciones para su uso son anafilaxia con la primera dosis y enfermedad aguda.
La utilidad de esta vacuna en poblaciones especiales todavía está en estudio. Aquellos pacientes con enfermedades crónicas, en particular insuficiencia renal crónica, diabetes mellitus, artritis reumatoide y psoriásica, y lupus eritematoso sistémico, tienen riesgo de casos graves de HZ, y aunque la medicación inmunosupresora podría, en teoría, montar una respuesta inmune silenciada a la vacuna, los principales beneficios de la prevención del HZ están apoyando la vacunación.
> Mujer de 80 años, por lo demás sana, consulta porque la semana previa había sido tratada por su médico por HZ en la parte superior del brazo izquierdo, y, mientras termina su curso de aciclovir, quiere saber si podría cuidar a su pequeña bisnieta. También quiere saber si podría "contraer" HZ con la vacuna como "contrajo" la gripe después de su última vacuna antigripal.
Las pautas de aislamiento para HZ reflejan la ubicación de la erupción, la edad y el estado inmunológico de cada paciente y sus contactos. En inmunocompetentes con presentación clásica, deben tomarse precauciones estándar (higiene de manos y protocolo respiratorio), y las lesiones deben ser protegidas hasta que estén secas y con costra.
Para los casos con distribución mucosa, principalmente trigeminal, aplican las mismas pautas. En este caso, las precauciones estándar mencionadas anteriormente son prudentes. Como su bisnieta es una bebé que no ha recibido ninguna dosis de vacuna contra VZV, estaría en riesgo de padecer infección por VZV de un paciente con HZ que está eliminando activamente el virus.
Sin embargo, considerando que la paciente no está inmunodeprimida y ha estado recibiendo tratamiento antiviral oral durante una semana, y que el área de erupción de HZ se cubre y se venda fácilmente, el riesgo de transmisión de VZV es insignificante. Por el contrario, en inmunosuprimidos, el VZV puede eliminarse más fácilmente, y quizás por períodos prolongados.
Los pacientes suelen preguntar sobre la infectividad de la propia vacuna para HZ. Con Zostavax, dentro de una ventana de 42 días, se han reportado erupciones "zosteriformes" en sitios de no inyección, consistentes con HZ de tipo salvaje incidental. Hay casos aislados del virus Oka de la cepa de vacuna Zostavax como fuente de HZ en pacientes inmunocompetentes, al igual que hay casos de HZ pediátrico de cepa Oka por la vacunación infantil para VZV, pero fuera de la ventana aguda de 1 a 2 meses.
Esto ocurre después de que la cepa HZ regresa a un estado latente en la raíz dorsal o en el ganglio del nervio craneal, y no es atribuible a una reacción aguda a la vacuna en sí. Esto es discutible ya que el uso de Shingrix supera al de Zostavax, y una vacuna recombinante no se somete a latencia o reactivación como lo haría una vacuna viva.
>Mujer embarazada de 32 años sana (32 semanas, primer embarazo) que nota un dolor "desgarrador" en el lado derecho del abdomen durante 2 días, seguido de un grupo de papulovesículas rosadas en esa zona y en la parte superior derecha de la espalda. Trabaja en una clínica ambulatoria. Su hermana también tuvo una erupción como esta durante el embarazo.
En teoría, la respuesta inmune de una mujer embarazada sana puede ser menos enérgica debido a la inmunidad celular materna compartida con el feto, por lo tanto, el HZ puede sobrevenir con mayor frecuencia que en las no embarazadas.
A diferencia de la verdadera viremia de la infección primaria por VZV, que ahora es más rara en EE. UU. debido a los exámenes prenatales de rutina para VZV, HZ no causa viremia con infección transplacentaria y los anticuerpos IgG protectores maternos específicos de VZV adquiridos por vacunación o infección primaria previa por VZV pasan entre madre y feto. Esto también, en teoría, protege al neonato si la embarazada desarrolla HZ cerca del momento del parto, pero las precauciones estándar antes mencionadas y el cuidado de las heridas aún estarían indicados.
En este caso de una trabajadora de la salud embarazada que desarrolla HZ, el miedo a la transmisión al feto se disiparía, ya que debería haberse sometido a una evaluación laboral para detectar la inmunidad al VZV mediante documentación del VZV infantil, vacunación contra el VZV o inmunidad de laboratorio.
Si el entorno del trabajador de la salud incluye personas que no son inmunes al VZV, en particular bebés o inmunosuprimidos, sería prudente una diligencia escrupulosa con las precauciones estándar. En este caso, dado que el área de HZ es una región del tronco que está cubierta constantemente, si cumple el tratamiento antiviral en la ventana adecuada, el riesgo de diseminación viral e infección para otros pacientes sería insignificante.
La terapia antiviral para el HZ en el embarazo se considera segura, y su inicio oportuno contrarresta la morbilidad grave, incluidos el dolor y las complicaciones de la herida, que podrían afectar negativamente el bienestar del feto.
En este caso, la hermana de la paciente también había desarrollado HZ en el embarazo, lo que puede reflejar una fuerte predisposición genética al HZ a lo largo de la ascendencia materna. Esto puede ser relevante para la vacunación contra el HZ en poblaciones fértiles más jóvenes a medida que continúan los estudios de vigilancia.
Actualmente, Zostavax está contraindicada en el embarazo. Para Shingrix, no hay datos que excluyan a las embarazadas de recibir la vacuna y, en teoría, su indicación de edad ≥ 50 años puede incluir una minoría de ellas. Se desconoce el riesgo de contacto durante la lactancia para un lactante de mujeres posparto que reciben cualquiera de las vacunas para HZ.
Resumen objetivo: Dra. María Eugenia Noguerol
Fuente:




No hay comentarios:
Publicar un comentario
Nota: solo los miembros de este blog pueden publicar comentarios.